�}�ᰢù���ڼ{���d�w����ʯīϩ�ϵĿɿ�ؓ�d�cጷ�
�������ø���Hummers���Ƃ�������ʯīϩ����̽�������������t�W��������{��ˎ���d�w�đ��á�ͨ�^������ʎ�ȷ����Ƃ�������ʯīϩ-�}�ᰢù��(GO-DXR)�����ø߷ֱ�����R(HRTEM)�������~׃�Q�t����V(FT-IR)������-��Ҋ�ֹ���V(UVVis)�Ȝyԇ������GO ؓ�dDXR ǰ�����ò�ͽY���M�����о���DXR ��GO �ϵ�ؓ�d�����_4.6mg/mg��DXR ��ጷ�����ͨ�^pH ֵ���ƣ��f��GO �cXR֮�g�������I���ýY�ϡ�
1������
�����S���{���g������ˎ�������lչ���{��ˎ���d�w�ɞ���T���о��I�{��ˎ���d�w���Ը�Чؓ�dˎ�������fˎ�P�ɿص�ጷ�ˎ����ҿ������Lˎ�����Õr�g���������������Լ���������С�ȃ��c���{��ˎ���d�w�ɷ֞�{�������{��֬�|�w���ۺ����z�����{�״����w������Ҋ�ļ{��ˎ���d�w��̼�{�ܡ���֬�|�w���F���w�������ӵȣ�����ͨ�^�������������I��Ƕ�����������ؓ�dˎ�
����ʯīϩ��һ�N���ж��S��C��Y�������ͼ{�ײ��ϣ������Ѓ��������W����W��늌W��W���ܣ��������tˎ�������������늻��W�ȷ�����Н��ڵđ��á��������һЩ�W��̽����ʯīϩ�������tˎ����đ��ã��e���������ˎ����f���棬ȡ����һ���ijɹ���ʯīϩ�����^��ıȱ���e������ͨ�^�����±��漰��߅��ؓ�dˎ�ؓ�d�����������{�ײ��ϸߺܶࡣ��ʯīϩ������������ʯīϩ�Y�����������Ȼ����u�����h�����F�����������ʯīϩ��ˮ���ԣ�ʹ����ʯīϩ�������������wѪҺ���ܽ⡢���ӡ�������n�}�M�о��˾��Ҷ������ļ{������ʯīϩ���鿹��ˎ���d�w��ͨ�^�ǹ��r�I��������ˎ��;ͬ�r�����ܻ�������ʯīϩ�������������Լ��o���ԣ����Ը�Ч��ؓ�d����ˎ����������о��˹��ܻ�������ʯīϩ�܉��Чؓ�d�ɷN����ˎ��������ٰ����������خ���;�ɷN����ˎ����ؓ�d���������a���^��Ķ��ԣ��Ķ�����Ч�ؚ��������������Ӣ�Ȉ��������ʯīϩ���Ը�Чؓ�d�}�ᰢù�أ�ͬ�r�ڲ�ͬpH ֵ�¿��Կ���ˎ���ጷţ��Ķ��_�����õ��t��Ч����
������ˣ������о����}�ᰢù��(DXR)������ʯīϩ(GO)�ϵĸ�Чؓ�d��ؓ�d�ʸ��������īI����������]�����wѪҺ���������ʣ������o�B��������ˎ���ڲ�ͬpH ֵ�µ�ጷš�ͬ�r�����üt����V�������Ҋ���V��DXR��GO �ϵ����������M���˷�����
2�������
����2.1������ʯīϩ���Ƃ�
����ͨ�^����Hummers���Ƃ�����ʯīϩ�����ȣ���69mL ��H2SO4 �м���1.5gNaNO3��3g��Ȼʯī��9gKMnO4�����ض��{����0�棬����һ�Εr�g���S��������35�棬���跴��1h��֮����138mLȥ�x��ˮ�����ߜض���98�棬�ټ���420mLȥ�x��ˮ��30mL�p��ˮ�������������Һ�M�П�V������5%���}����ϴ���õ�����ʯī��������ʯī����ˮ�в���1.5h���x��ȡ�ό�Һ�w���ٴ�����һ�������}���У��x�ĵ��ӳ�������65���¸���24h��������ʯīϩ��
����2.2���}�ᰢù��(DXR)������ʯīϩ(GO)�ϵ�ؓ�d
�����Q��һϵ�в�ͬ�|����DXR ����0.16mg/mL��GO ��Һ�У���1h���ںڰ��l��������ʎ���Ϸ���12h��������Һ��14000r/min�¸����x��1h��ȡ�ό���Һ��ͨ�^�����Ҋ�ֹ���Ӌ��485nm ̎�y��������ȣ��Ķ����Դ_������Һ�ĝ�ȣ�Ӌ���DXR ��GO �ϵĆ�λؓ�d������λؓ�d��Ӌ�������ʽ(1):

����2.3���}�ᰢù��������ʯīϩ�ϵ�ጷ�
����ȡijһ��ȵ�9mLGO-DXR��Һ��������֞�3�ݣ����������У��քe����80mLpH ֵ��4.00��6.86��9.18�����ᾏ�_��Һ�У��o�ã���1d���S���ڲ�ͬ�r�g�c�y������Һ������ȣ��Ķ�Ӌ���DXR��ጷ�����ጷŰٷ�����Ӌ�������ʽ(2):
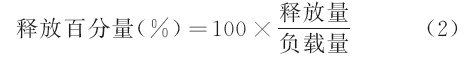
����2.4���^�Y������
����ͨ�^�߷ֱ�������@�R(HRTEM��JEOL3010)���Ƃ��GO ��GO-DXR�ĽY���ͱ�����ò�M�б������üt����V�x(FT-IR��NicoletNexus670)������-��Ҋ�ֹ���Ӌ(UV��TU1810)����Ʒ�ĽM���M�з�����
�YՓ
����(1)�����ø���Hummers���Ƃ�������ʯīϩ��ͨ�^���γ�����ʎ�ȷ������}�ᰢù��ؓ�d������ʯīϩ��;��ͨ�^�t����V������-��Ҋ���V������֪���}�ᰢù���c����ʯī֮�g�����Þ���I������
����(2)���}�ᰢù��������ʯīϩ�ϵ�ؓ�d���^�����{�ײ��ϸߺܶ࣬��ؓ�d�����_4.6mg/mg���������ʯīϩ�ڼ{��ˎ���d�w������Н��ڵă��ݡ�
����(3)��GO-DXR�ڲ�ͬpH ֵ���o�B����ጷ���r�������}�ᰢù�������ԗl���µ�ጷ�����ߣ������[��������pH �ĭh�����Ķ��������t�W�������ڿ���ˎ���ጷš�