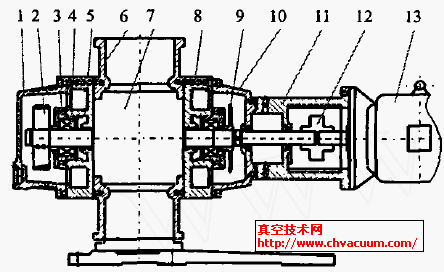
ˮ���������l�����Y
����ˮ��һ���ĉ����¼ӟ��_��ij���ضȣ�������c�ضȻ�Q͜ض�Ts �rˮ���_ʼ���v���_��͜ضȵ�ˮ�Q�ˮ���^�m�ӟ�ˮ����u�������@�rˮ�������Ĝضȱ��ֲ�׃��ˮ��ȫ׃�������r���ض��Ա��ֲ�׃���@�r�������Q����������������ˮ߀�]��ȫ׃�������֮ǰ���ˮ����������棬�@�r�������Q������������Q�������������������ټӟᣬ�����ض��_ʼ�������@�r�����Ĝضȳ��^͜ضȣ��˕r�������Q���^���������ڲ�ͬ�ĉ����£�ˮ��͜ض�Ҳ��ͬ�����Y��������ˮ��͜ض��S��������߶�������ֻ���ژ˜ʴ�≺��760��×133 Pa)�£�ˮ�ķ��c�ضȲ���100�棬�������ĉ�����ˮ��͜ضȿɲ���@�á�
�������O��һ���������b�Mһ������ˮ�����b�M����Ȼ������������ˮ���Ϸ��Ŀ՚���ߣ������������]���՚�����ˮ���Ϸ�����������ՠ�B�����dz�M��ˮ��������ˮ���l���ã���ˮ��������̎���Ɂy�ğ��\���У��������ײ����ˮ����ײ���ں�ˮ����ײ�r���е���Ȼ�������еľ͵��Mˮ��׃��ˮ���ӡ�ˮ�����ĉ��������چ�λ�r�g�ȵ��Mˮ���ˮ�������ӵĔ�Ŀ�����ࡣ��һ���棬������ˮ�ķ���������ͣϢ�ğ��\�ӣ�ˮ�渽�������^���ˮ�����п��ܒ�Óˮ�棬׃��ˮ�������ӡ�ˮ�Ĝض����ߣ������\�������ң��چ�λ�r�g��Ó�xˮ��ķ��Ӿ����ࡣ��һ���ض��£�ˮ�����ĉ��������Ԅӷ�����һ����ֵ�ϣ��@�r�M��ˮ���Ó�xˮ��ķ��Ӕ���ȣ�ϵ�y̎��ƽ���B��Ҳ�������^��͠�B��͠�B�µ�ˮ�Q�ˮ��͠�B�µ�ˮ�����Q�ˮ������������ĉ����ɞ�͉���Ps���Һ�w������������Ĝضȳɞ�͜ض�Ts����׃͜ضȣ�͉���Ҳ��������׃����һ����͜ضȿ��nj�����һ����͉�����һ����͉������nj�����һ����͜ضȡ�͜ض����ߣ�͉���Ҳ���ߡ�
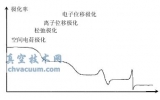
�����Ɍ����Ԝy��͜ض��c͉������Pϵ����D1 ��ʾ�����ضȳ��^һ���Ĕ�ֵtK �r��Һ�Bˮ�����ܴ��ڣ���ֻ������ˮ������tK �Q���R��ضȡ��c�R��ضȌ�����͉���PK �Q���R�牺���������R��ضȺ��R�牺������ߵ�͜ضȺ�͉�����ˮ������ˮ���������R���B����ֵ�飺

��������������һ���Ĕ�ֵPA �r��Һ�BˮҲ�����ܴ��ڣ���ֻ����ˮ�������߱���PA �Q�������c�������c�����c����������͜ض�tA �Q�������c�ضȡ����������c�����������c�ض�����͵�͉�����͜ضȡ�ˮ�������c�ضȺ������c�����飺

����ʹ1 kg ���ˮ��һ�������£���ȫ׃����ͬ�ضȵ��ˮ�������������ğ����Q��ˮ���������ᣬ�÷�̖r ��ʾ�����Ć�λ��kJ/kg��
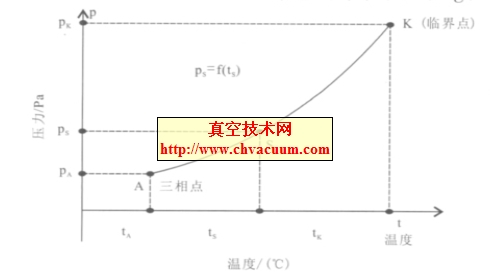
ˮ�������c���Y
������Һ�w�ăȲ��M���������^�̷Q����v���������һ���l�����M�С����Ĝض�t Ҫ��͜ض�tS �Ը�һЩ����Һ�w���̎���^�����r�²��ܷ��v���^���Δt=(t- tS)Խ�ߣ��t���v�����ҡ���Һ�w�����M���������^�̷Q�����l�����l���κΠ�B�¶����M�С�
�����������c�ض�t ����͜ض�tS �ı�����|�r�����͕��ڱ��������Y��Һ�w��������Һ�w��Һ�w�����w����ĸ���������Һ�w�ܷ�������P��߅��θ��90°��Һ�w����������Һ�w����ˮθ=50°�� ���������Y�r���ڱ������γ�������ҺĤ������s����������_���������Y�r���ų��ĝ�����Ҫͨ�^ҺĤ���܂��o���棬Ĥ�����Y�r��������������Ӱ푣����Y��Һ�w������s���������\�ӡ��������л��s�՚�������������Y�Ě��w�r�����Y�ş��Ҫ�ܵ�Ӱ푣����ֻ�������������Y��������ϣ����՚��Ԍ����֚�B���e���ڱ��渽������ֹ�����������ĔUɢ����Ӱ푓Q��Ч��������ձ������⣬�՚��Ӱ푕����pС��