��ռ��g(sh��)�Ўׂ�(g��)��Ҫ�ĸ���
����һ��(g��)��≺�£��՚�ķ����ܶ�n=2.7×1019��(g��)/cm3��
�����՚��ǻ�Ϛ��w��������(du��)�����|(zh��)���ɘ�(g��u)�ɵĚ��w���Ӱ�����Ӌ(j��)�㡣��?d��)�����?du��)�����|(zh��)��28.016���w�e��78.1%;���������(du��)�����|(zh��)��32���w�e��20.93%;��������(du��)�����|(zh��)��39.944���w�e��0.933%��
����(du��)�����|(zh��)����ƽ��ֵ=(28.016×78.1+32×20.93+39.944×0.933)/(78.1+20.93+0.933)=28.96
�����ɚ��w�����\(y��n)��(d��ng)Փ������(qi��ng)��Ӌ(j��)��ʽ��
p=nkT
�������Ç�(gu��)�H��(bi��o)��(zh��n)��λ�r(sh��)(����(qi��ng)Pa���w�e m3)������Ɲ������(sh��)k��1.38×10-23 J/K��
�������w���ӵ��ܶȞ�
n=p/(kT) (1-4)
��������(qi��ng)��1Pa���ضȞ�27��r(sh��)�����w���ӵ��ܶ�n��
n=1/(1.38×10-23×(273+27))=2.4×1020��(g��)/m3
������ˣ���ʹ��ն��_(d��)��10-9 Pa�ĘO����ՠ�B(t��i)��ÿ�����Ŀ��g��(n��i)����1011��(g��)���w���Ӵ��ڡ�
1�����w���ӵ�ƽ�����ɳ�
�������w���ɴ����ķ��Ә�(g��u)�ɵģ�0��һ��(g��)��≺����r�£�22.4L�Ŀ��g����1Ħ��(6.02×1023��(g��))���ӡ��@Щ�������Ҝ�����500��1500m/s���ٶ��\(y��n)��(d��ng)������������ײ��׃�\(y��n)��(d��ng)������ٶȣ�֮���ٺ�����ķ�����ײ���ɴ���ײ֮�g���w�о��x���Q֮��ƽ�����ɳ̡�
����ƽ�����ɳ�λ[m]������(qi��ng)p[Pa]���ض�T[K]�Լ����ӵ�ֱ��D[m]֮�g���P(gu��n)ϵ��
λ=3.11×10-24 T/pD2(1-5)
������ˣ����w���ӵ�ƽ�����ɳ��c����(qi��ng)�ɷ��������c�ضȳ����������c����ֱ����2�η��ɷ������P(gu��n)ϵ��
�����ضȞ�25��Ŀ՚⣬����(qi��ng)�ͷ���ƽ�����ɳ̵Č�(sh��)�H��(sh��)��(j��)��1Pa��7mm��10-1 Pa��7cm��10-2 Pa��70cm��10-3 Pa��7m��10-4 Pa��70m��ӛס�@Щ��(sh��)�֣���(du��)��նȵĸ��X(ju��)�ܸ�ֱ�^һЩ��
2�����w���ӵ������l��
�������w�����چ�λ�r(sh��)�g�͆�λ��e��(n��i)��ײ���w����Ĕ�(sh��)���Q֮�������l�ʡ������l��r�͉���(qi��ng)p[Pa]�����w����(du��)�����|(zh��)��Mr���ض�T[K]֮�g���P(gu��n)ϵ��ʾ��
r=2.6×10-24 p/(MrT)1/2[��(g��)/(m2·s)] (1-6)
�����������l�ʺ͉���(qi��ng)�����������͚��w����(du��)�����|(zh��)��ƽ�������ضȵ�ƽ�����ɷ������P(gu��n)ϵ��
��������ն���10-4 Pa����r�£�25�������ӵ������l����2.72×1018 ��(g��)/(m2·s)�������ڹ��w�����ԭ�Ӕ�(sh��)��s��1019 ��(g��)/m2��ֻҪ����犵ĕr(sh��)�g���������е�ԭ�Ӷ���(hu��)�ܵ������ӵ���ײ��
����������w���ӵ�ƽ�����ɳ̺������ijߴ���ͬ����L(zh��ng)���t���w���Ӻ���������ײ�ĴΔ�(sh��)Ҫ�Ț��w����֮�g����ײ�Δ�(sh��)Ҫ�࣬�@�N��B(t��i)���Q�������(�D1.3(a))�����ƽ�����ɳ̱��^�̣����w����֮�g����ײ�Δ�(sh��)�Ț��w���Ӻ������ڵ���ײ�Δ�(sh��)�࣬�@�N��B(t��i)���Q�������(�D1.3(b))��������Ě��w�����ڹ�·�б��ų��r(sh��)�������S������������ܱڵ�������u�pС��
����ᘌ�(du��)����������������@����Օr(sh��)Ҫ�x��ͬ��͵���ձã��@���Ժ���ձ�һ��(ji��)�Ќ���(hu��)Ԕ��(x��)��B��
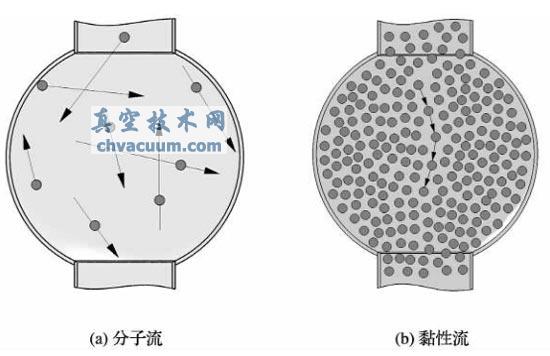
�D1.3�����������������ʾ��D
3������еğ����(d��o)
�������g�Ѓɂ�(g��)λ��������ڜضȲ�t��(hu��)�l(f��)�������(d��o)�����w���Ӟ����������r������(qi��ng)׃�����f�����ķ����ܶȺͷ��ӵ�ƽ�����ɳ�Ҳ�l(f��)��׃�������ڷ��ӵ�ƽ�����ɳ̺ͷ����ܶȌ�(du��)�����(d��o)��Ӱ������෴�����ã���ˣ���(du��)�������(l��i)�v�����w��(du��)�����(d��o)��ؕ�I(xi��n)�͉���(qi��ng)���P(gu��n)ϵ�ɺ��Բ�Ӌ(j��)��
�������w���Ӟ����������r��������w���ӵ�ƽ�����ɳ̱���Ճɂ�(c��)�g��߀�L(zh��ng)���@�ß��ܵĚ��w���ӌ�ֱ�Ӵ��^(gu��)��ն��\(y��n)��(d��ng)����һ��(c��)����ˣ�ͨ�^(gu��)���w���ӂ��f�ğ����͚��w�ķ����ܶ����P(gu��n)�����w�ķ����ܶȺ͉���(qi��ng)�������������Ԛ��w���ӂ��f�ğ����͉���(qi��ng)�������������ǣ�̎�ڷ������ķ����ܶȷdz��ͣ���(sh��)�H�ğ����(d��o)Ҳ�ɺ��ԡ�
������(du��)��խh(hu��n)����(l��i)�f(shu��)����������B(t��i)�ğ����(d��o)��Ҫ��ݗ�䡣������������M(j��n)�б�Ĥ���L(zh��ng)�r(sh��)��������߱�Ĥ�|(zh��)����ͨ��Ҫ��(du��)�r���M(j��n)�мӟᣬ�ӟ���Ҫ�������ß�ݗ���(l��i)��(sh��)�F(xi��n)��